Anvisa retira obrigação de fase 3 no Brasil para autorizar vacina
Esta é a principal mudança trazida na atualização do guia para uso emergencial de imunizantes contra a Covid-19.
Nesta quarta-feira (03), a Agência Nacional de Vigilância Sanitária (Anvisa) anunciou o fim da exigência de estudos da fase 3 em andamento no Brasil para autorização emergencial de vacinas no país. Esta é a principal mudança trazida na atualização do guia para uso emergencial de imunizantes contra a Covid-19.
O prazo de análise para vacinas sem estudo de fase 3 desenvolvido no Brasil será de até 30 dias. O guia passa a contar com a seguinte redação: "A vacina deve preferencialmente possuir um Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) anuído pela Anvisa e o ensaio clínico fase 3, pelo menos, em andamento e em condução no Brasil".
- Foto: Divulgação
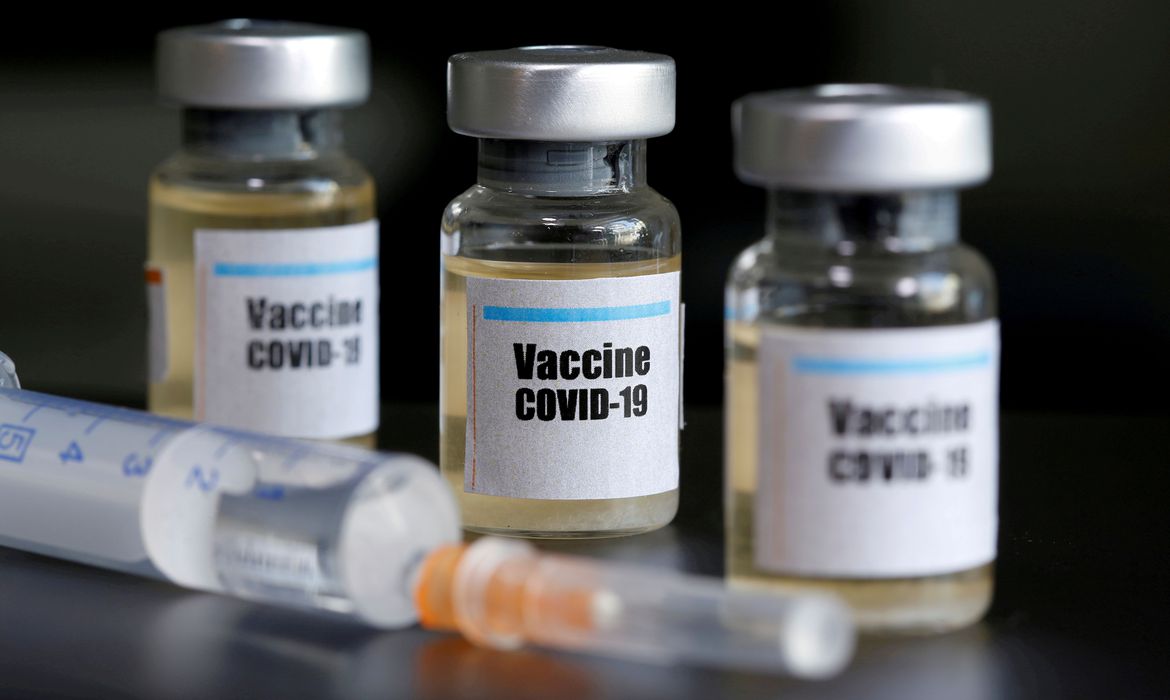 Produção de Vacina contra Covid-19
Produção de Vacina contra Covid-19
Com a mudança, a norma da Anvisa segue exigindo estudo de desenvolvimento clínico da vacina na fase 3, mas agora ele não precisa estar sendo conduzido no Brasil. São os estudos da fase 3 que mostram o percentual de eficácia da vacina, quantas doses devem ser aplicadas, além da avaliação de eventuais reações adversas.
"Essa atualização faz parte da estratégia regulatória do Brasil de favorecer acesso. Ela está apartada de qualquer discussão que seja fora do âmbito técnico, para que o Brasil garanta que tenha acesso a vacinas com qualidade, eficácia e segurança", disse a diretora da Anvisa, Meiruze Freitas, durante coletiva de imprensa para comunicar as alterações.
No caso de fase 3 realizada no exterior, caberá ao laboratório requerente apresentar os dados brutos do estudo, fazer o acompanhamento dos participantes dos testes para avaliação de eficácia por, pelo menos, um ano e apresentar demonstração de que os estudos pré-clínicos e clínicos foram conduzidos conforme as diretrizes aceitas nacional e internacionalmente.
"A vacina com estudo de fase 3 aqui no Brasil ou no exterior vai ter que seguir o mesmo critério de segurança, qualidade e eficácia. A única diferença vai ser a necessidade de apresentar dados que permitam que nós tenhamos confiança no estudo no exterior e que esse estudo mostre que a vacina serve para a população brasileira. E nós como agência reguladora vamos assegurar isso", afirmou Gustavo Mendes, gerente-geral de medicamentos da Anvisa.
Até agora, no Brasil, existem duas vacinas com autorização de uso emergencial: a Coronavac, desenvolvida pelo Instituto Butantan em parceria com a Sinovac; e o imunizante desenvolvido pela farmacêutica AstraZeneca, em parecia com a Fundação Oswaldo Cruz (Fiocruz).
A flexibilização nas regras do pedido de uso emergencial pode beneficiar, por exemplo, o laboratório União Química, que está à frente da produção da vacina russa Sputnik V no Brasil. O imunizante ainda aguarda autorização de estudo fase 3 no país, mas agora não dependerá mais desse pré-requisito para encaminhar o pedido.
De acordo com Meiruze Freitas, a expectativa é que a nova redação do guia para uso emergencial amplie a oferta de vacinas no país. "A gente ainda não recebeu isso diretamente de nenhuma empresa, mas eu espero fortemente que tenha impacto. Isso certamente possibilitaria para a Moderna, Novavax e um monte de outras vacinas, dentro inclusive do portfólio da Covax Facility ".
-
Ministério da Saúde aponta que vacinação com Pneumo 20 começa em duas semanas pelo SUS
Conforme o Ministério da Saúde, o imunizante protege contra 20 sorotipos da bactéria Streptococcus pneumoniae, principal causadora de doenças graves como pneumonia e meningite. -
Saiba como fazer a prevenção de cinomose canina nos pets
O imunizante, Vanguard Plus, utilizada contra a cinomose e outras doenças está disponível na Clínica-Escola da UNINASSAU Jockey. -
Esperantina alerta para vacinação contra a gripe de pessoas com doenças crônicas
As autoridades de saúde reforçam o apelo sob o lema de que "A vacinação salva vidas!", incentivando os cidadãos a garantirem sua dose para a proteção individual e coletiva de toda a comunidade. -
Hospital Regional Tibério Nunes contará com mais de 300 leitos após obras em Floriano
Conforme a Sesapi, os investimentos em estrutura e ampliação dos serviços ultrapassam R$ 18 milhões. -
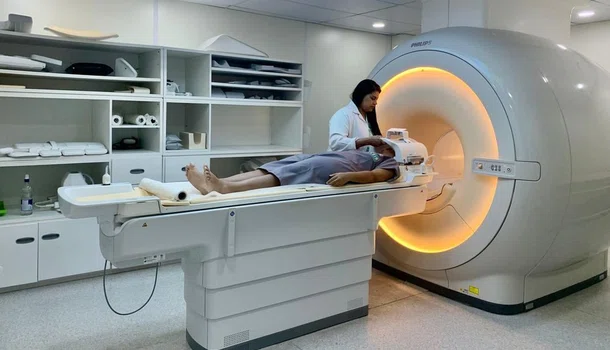
Mais de 20 municípios do Piauí são beneficiados com Carreta de Ressonância Magnética
De acordo com a Secretaria de Estado da Saúde do Piauí (Sesapi), o projeto do Ministério da Saúde garante acesso a exames especializados.








E-mail
Messenger
Linkedin
Gmail
Tumblr
Imprimir